放疗响应药物领域获得新进展 |
 |
来源:网络 2024-05-01 13:55
该工作基于有机光致电子转移(PET)原理开发出一种新型、高效的放疗射线响应的基团,并成功应用于抗体偶联药物(ADC)的设计中,解决传统ADC药物脱靶及释放效率低的问题。北京大学化学与分子工程学院应用化学系刘志博团队致力于开发放疗特异性响应的保护基团,并应用于化疗药物的前药设计中,以放疗介导的肿瘤部位化疗药物、可控释放,解决临床联合治疗中减毒增效的临床问题。
刘志博团队在Nature Chemistry期刊上发表了题为的新研究(图1)。该工作基于有机光致电子转移(PET)原理开发出一种新型、高效的放疗射线响应的基团,并成功应用于抗体偶联药物(ADC)的设计中,解决传统ADC药物脱靶及释放效率低的问题,初步验证了放疗响应药物技术在ADC药物设计中的应用潜力。论文共同第一作者是傅群峰博士,博士研究生顾郅、申思涌;通讯作者是刘志博。
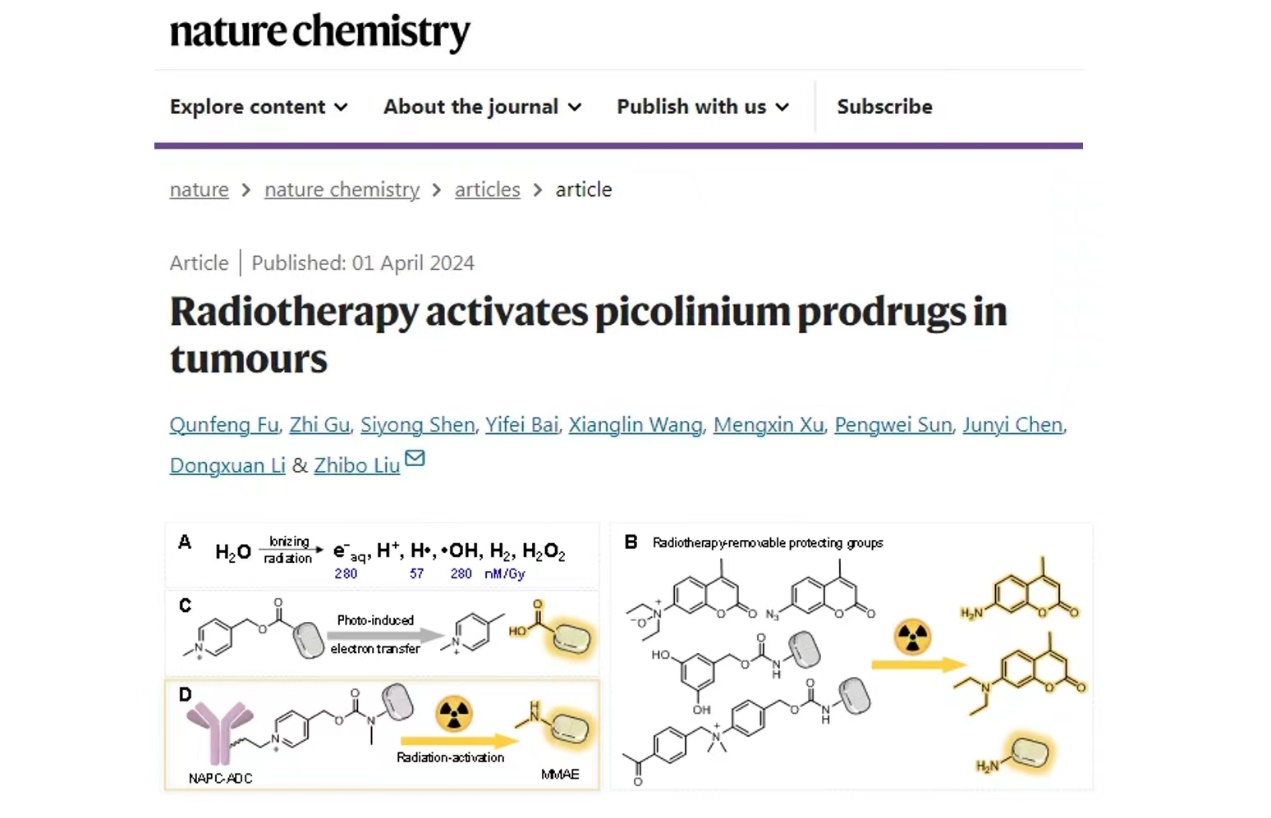
图1:放疗激活NAPC前药释放功能分子
在光致电子反应中,光敏剂接受光照后产生光电子参与化学反应。考虑到辐射产生的水合电子和光电子的相似性,研究团队通过设计筛选出反应基团NAPC,在辐射条件下实现高效脱除,并系统研究了取代基位置和电子密度对反应基团辐射还原效率的影响,提出辐射介导释放的反应机制。与已报道的放疗响应基团相比,NAPC是迄今为止效率最高、选择性最好的放疗响应基团(图2)。

图2:筛选得到有最高反应效率的放疗射线响应基团
研究人员将所开发的NAPC放疗响应策略应用于ADC药物,以适配ADC药物的精准控制释放策略,解决ADC开发中有效载荷递送脱靶和释放效率低的问题。NAPC-ADC联合X射线治疗组在抑制肿瘤生长方面表现出显著优势,且未表现出明显的副作用(图3)。
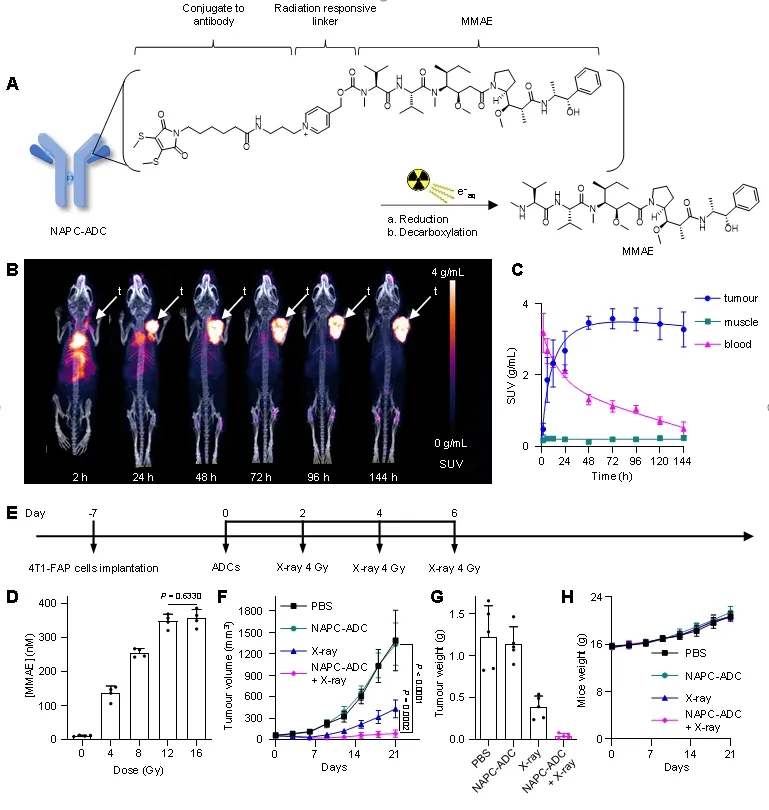
图3:NAPC放疗响应策略应用于ADC药物
该工作填补了从光化学到辐射化学领域过渡的技术空白,进一步扩充了放疗射线响应的活性基团范围。同时,刘志博团队正在从分子成药性、安全性、有效性及临床放化疗方案的适配性出发进行放疗响应药物的开发迭代与临床转化研究,有望开辟领域的新范式。
该项工作得到了北京大学化学与分子工程学院、北京分子科学国家研究中心、昌平实验室、北大-清华生命科学联合中心、国家杰出青年科学、中华人民共和国科学技术部、北京市的资助。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 科研人员研发新探针实现对固定细胞线粒体的STED成像 (2024-05-17)
- Neuron:科学家识别出人类多系统萎缩症的四种新型的遗传风险因素 (2024-05-16)
- Mil Med Res (2024-05-16)
- 《自然·通讯》:武汉大学团队发现,免疫细胞释放的特定外囊泡竟会助长肿瘤气焰! (2024-05-16)
- GUT:科学家首次发现,早老素缺失或是AD和肠炎的共同病因! (2024-05-16)
- Cell:新型mRNA癌症疫苗,只需一针,在人类脑肿瘤患者中迅速激活抗肿瘤免疫反应 (2024-05-16)
- 上海交通大学医学院研究者们创造"合成生物学创造奇迹:细菌囊泡携带BMP (2024-05-15)
- Nat Biotechnol (2024-05-15)
- J Extracell Vesicles:细胞凋亡囊泡是修复DNA损伤和抑制细胞过早衰老所必需的 (2024-05-15)
- 眼科药物创新前沿论坛 (2024-05-15)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















