Nature系列综述:罗伯特·兰格概述黏膜疫苗设计中工程材料的作用 |
 |
来源:生物世界 2023-12-25 11:23
尽管黏膜疫苗有了实质性的发展,但目前只有少数疫苗(其中大部分是口服疫苗)获得了FDA的批准。黏膜疫苗的开发在递送、接种、免疫原性和安全性等方面面临独特的挑战,需要根据不同给药途径或接种黏膜部位,以及不Robert Langer等人在Nature旗下综述期刊Nature Reviews Materials上发表了题为:The role of engineered materials in mucosal vaccination strategies的综述论文。
该综述按给药途径分类,概述了当前黏膜疫苗的材料设计在克服现有给药挑战上的重要性。

据报道,有超过90%的病原体通过黏膜部位进入人体。黏膜病原体在黏膜组织中复制并通过接触黏膜分泌物传播。因此,设计直接在黏膜部位产生保护的疫苗接种策略有助于更好地预防感染、限制疾病严重程度和减少流行病传播,能够在病原体进入点直接靶向和中和病原体。
道(包括口腔、食道、胃、小肠、结肠、直肠)具有较大的表面积,是所有黏膜组织中被研究最多的组织。另一方面,呼吸道(、气管、肺)是的首要组织。虽然与道和呼吸道相比,女性生殖道(子宫、阴道)的表面积较小,但却是性传播疾病常见的感染部位。下表总结了常见黏膜感染病原体及其感染途径(呼吸道、胃肠道或泌尿生殖道)、死亡和感染人数以及目前的疫苗覆盖率。
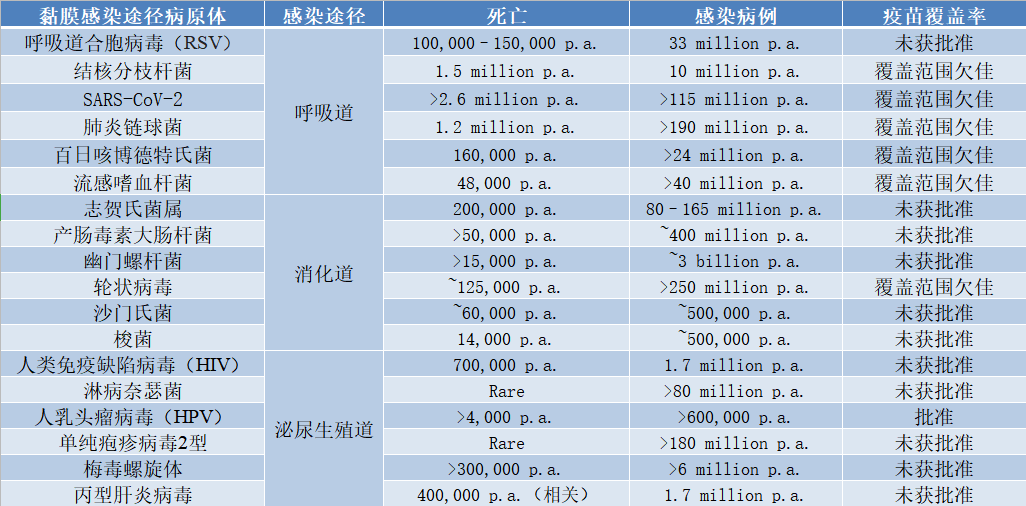
表1. 常见黏膜感染疾病及防控现状
然而,黏膜组织的许多特征对疫苗递送提出了挑战。除了物理屏障外,黏膜具有抑制微环境、可变pH和多样化的微生物群,能够快速清除、降解外源性物质。因此,黏膜疫苗无论免疫原性成分如何,均需要防止被表层黏膜组织降解,抵抗机械清除并穿透黏液层,直到疫苗到达靶点位置并被适当的细胞群吸收,继而由免疫原性抗原呈递细胞(APC)呈递激活免疫。目前已开发多种功能迥异的生物材料,能够在防止免疫原性成分降解、实现定位、靶向细胞群、pH值响应释放和动力学以及实现佐剂效果等方面发挥独特作用,使得不同功能的生物工程材料成为了改进黏膜疫苗的理想平台。
黏膜免疫最突出的指标之一是黏膜中免疫球蛋白A(IgA)的产生。然而,全身途径产生的IgA不会转运到黏膜分泌物中。一些疫苗可能会引起可测量的血清 IgA,但可能不会同时引起黏膜IgA的产生。对病原体的有效保护需要全身和黏膜免疫反应的协调参与,同时产生免疫球蛋白G(IgG)和IgA抗体。因此本综述中将IgA和IgG的产生作为疫苗有效性的衡量标准。 了解黏膜组织结构和特性 为了配制有效的黏膜疫苗,了解黏膜组织的结构和特性至关重要。黏膜组织是人体与周围环境之间的屏障,可分为I型和II型(图1a,b)。 I型黏膜包括胃肠道、呼吸道和女性上生殖道的组织。I型黏膜组织内衬有一层柱状上皮细胞,除了通过新生儿Fc受体(FcRn)转运IgG外,还表达聚合物免疫球蛋白受体(pIgR)通过上皮转运IgA进入固有层。分泌型IgA(sIgA)通过pIgR-IgA复合物的裂解释放到I型黏膜的管腔中。黏膜相关淋巴组织(MALT)是继发性淋巴组织,主要存在于I型黏膜组织中,其中微折(M)细胞从黏膜表面吸收抗原从而激活幼稚T细胞和B细胞。 II型包括角膜、口腔、食道和女性生殖系统的组织。II型黏膜组织内衬为分层鳞状上皮细胞,仅表达FcRn转运IgG。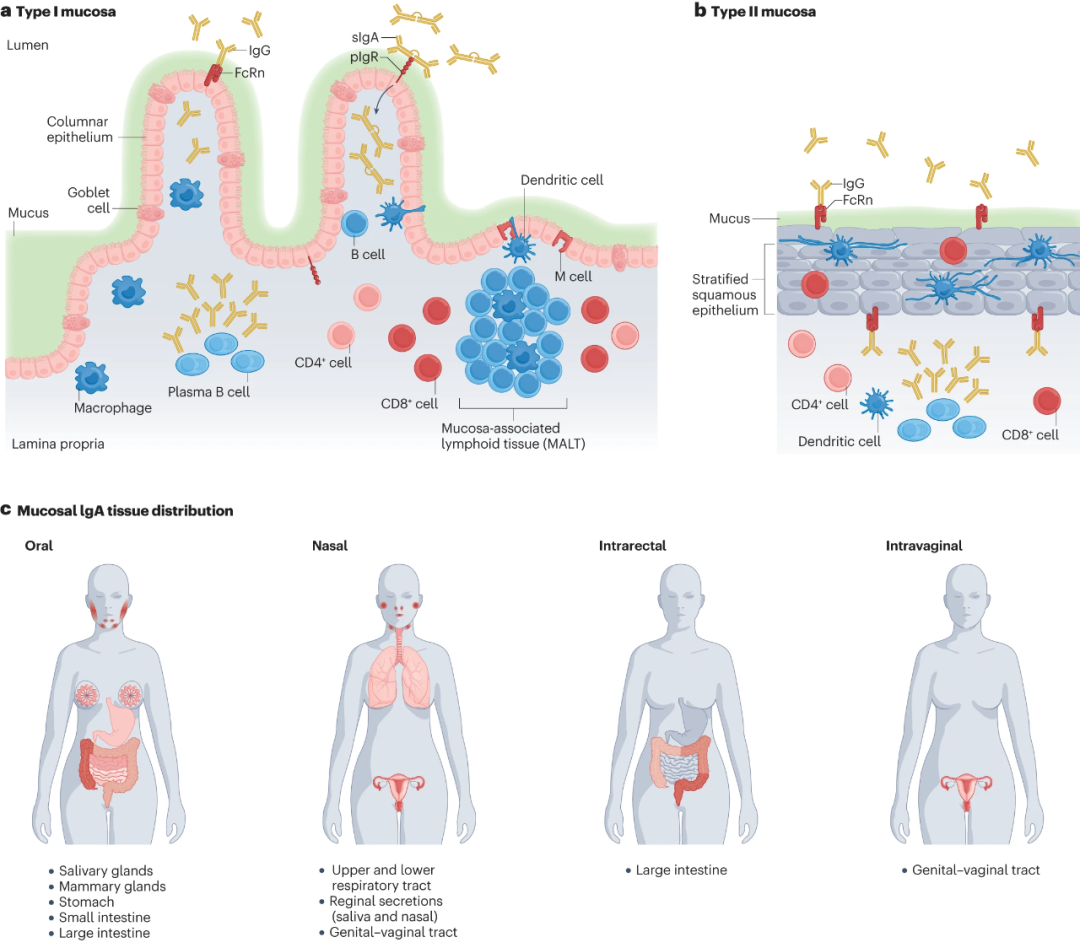
图1. I型和II型黏膜组织以及黏膜组织IgA分布
不同给药途径接种疫苗后黏膜组织IgA分布如图1c所示。通常IgA保护以一种固定模式表现:其中直接接触疫苗的黏膜处反应最强,其次是在邻近黏膜处的反应。有研究发现,在远端黏膜组织中可以诱导免疫反应,例如鼻内给药后阴道和直肠组织中IgA的产生。远端黏膜免疫的强度通过不同级别的阴影来描述(阴影越深表示响应越强)。
无论具有何种表面形态,黏膜组织都有共性的结构划分,可以细分为三个不同的结构层:黏液层、上皮层和固有层,固有层是位于上皮层下方的组织层,由基底膜隔开。尽管多层黏膜组织结构可以防止病原体入侵,但它们也是疫苗设计中必须克服的障碍。此外,黏液的运动和脱落,得益于呼吸道中纤毛上皮的摆动或胃肠道的蠕动,影响疫苗制剂的扩散。因此,为了开发有效刺激黏膜组织保护性免疫反应的黏膜疫苗,必须了解黏膜组织的特性。黏液层由I型杯状细胞(Goblet Cell)和II型黏膜组织中的邻近腺体分泌的水合黏蛋白网络组成,充当第一黏膜屏障限制病原体进入上皮层。黏液层的厚度在不同的黏膜组织中差异很大,在同一组织也各不相同。因此在设计黏膜疫苗时,应考虑给药部位的黏液层厚度,以及对疫苗进入上皮层的影响。
上皮层作为第二层黏膜表面屏障,厚度范围为100至800 m。I型黏膜组织的上皮层由简单的柱状上皮和分泌黏蛋白的杯状细胞组成。然而,II型黏膜组织中的上皮层由分层鳞状上皮细胞和多层角质形成细胞组成。与I型组织中的单细胞层相比,II型组织中的这种多层细胞结构提供了更好的机械应力保护。这种结构差异表明,疫苗制剂需要更深入地渗透到II型黏膜组织中,才能穿过上皮层到达固有层以激活免疫细胞。
固有层包含大量的树突状细胞、巨噬细胞以及复杂的血液和淋巴管系统网络。破坏上皮细胞的抗原可以被树突状细胞吸收,并通过收集淋巴管带到引流。黏膜相关淋巴组织(MALT)包含相当一部分CD8 T细胞、 T细胞和抗原采样微折(M)细胞,它们跨越覆盖B细胞和T细胞滤泡的上皮细胞到固有层。淋巴细胞活化在MALT中通过M细胞取样和腔内抗原的转胞吞作用发生,然后由树突状细胞呈递给MALT中的幼稚淋巴细胞。MALT可进一步细分为肠道相关淋巴组织(包括肠Peyer和孤立的淋巴滤泡)、鼻相关淋巴组织(包括人类的扁桃体)和诱导型支气管相关淋巴组织。黏膜表面具有一定丰度的经历抗原的组织驻留淋巴细胞,为对抗黏膜病原体提供了强大的局部保护。
黏膜给药途径与材料策略
黏膜疫苗递送具有多种材料设计和装置,例如胶囊、粉末、喷雾剂、乳膏、液体(乳剂、溶液和混悬液)和微针贴片等(如图2)。此外,根据疫苗免疫原性成分(即DNA、mRNA、、灭活病毒等)的化学性质,需要对疫苗递送载体的理化特性进行定制,以帮助有效成分的封装和递送。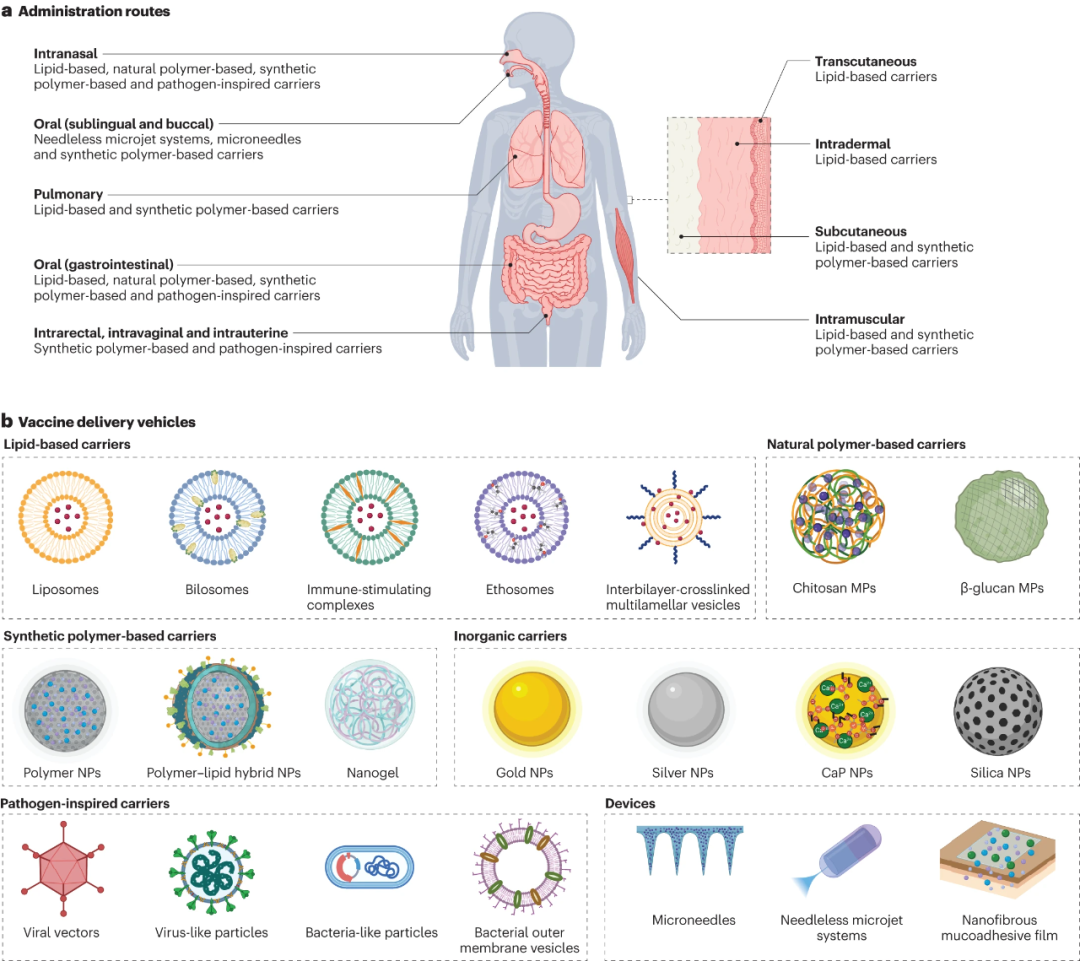 图2. 常见黏膜疫苗接种途径和递送材料
医药网新闻
图2. 常见黏膜疫苗接种途径和递送材料
医药网新闻

- 相关报道
-
- Nature子刊:新研究发现表达嵌合抗原受体的MSC细胞有望治疗一系列自身免疫性疾病 (2024-04-28)
- Nature:科学家揭示人类大脑前脑发育的奥秘 (2024-04-28)
- 亚马逊发表Nature Medicine论文,用大语言模型减少线上药店用药错误 (2024-04-28)
- Nature:新研究发现小RNA结合蛋白La可提高先导编辑效率 (2024-04-28)
- Nature:中外科学家构建出迄今为止最全面的人类衰老骨骼肌的单细胞图谱 (2024-04-28)
- Nat Immunol:利用机体B细胞通过靶向作用线粒体代谢来抵御人类癌症或自身免疫性疾病 (2024-04-28)
- Cell子刊:这个人体中的天然基因突变,能够预防脂肪肝和肥胖 (2024-04-28)
- 《柳叶刀》子刊:这些食物吃了易得糖尿病!12万余人近12年随访证实,高升糖指数饮食与2型糖尿病风险增加15%有关 (2024-04-28)
- Redox Biology:ALOX15B通过脂质过氧化、ERK1/2和SREBP2控制巨噬细胞胆固醇稳态 (2024-04-27)
- JCO:科学家有望开发出治疗人类白血病早期复发的新型联合疗法 (2024-04-27)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















